Рвота при спинальной анестезии

Появившись еще в середине девятнадцатого века, наркоз стал прорывом для медицины. До его открытия многие заболевания, такие как аппендицит, острый холецистит, проникающие ранения были для человека смертельными. В настоящее время анестезия позволяет делать операции любой сложности, спасая миллионы жизней ежегодно.

При помощи наркоза ежедневно проводят огромное количество операций безболезненно для пациента
Основная цель анестезии – выключение болевой чувствительности и автоматических неврологических рефлексов, развивающихся в ответ на боль и повреждение тканей (тахикардия, изменение кровяного давления, сужение периферических сосудов), что позволяет делать необходимые манипуляции.
Виды анестезии
- Местная. Применяется при локализованных патологических процессах кожных покровов и слизистых. Анестезия может быть поверхностной и инфильтративной, в зависимости от необходимой глубины вмешательства.
- Проводниковая. Позволяет выключить боль по ходу нервного ствола, и делать более масштабные операции без наркоза. Современные методы проводниковой анестезии: эпидуральная и спинномозговая. Они помогают отключать болевую чувствительность целых конечностей, а также брюшной полости и полости малого таза, и делать полостные операции, а также операции на суставах, не выключая сознания пациента.
- Наркоз. Общая анестезия отключает болевую чувствительность, а также рефлекторный автоматизм всего тела человека, позволяя делать сложные и длительные операции. Именно благодаря наркозу развиваются новые высокотехнологичные операции и методы лечения.
Для любого вида анестезии необходимы препараты, действующие на нервную систему и блокирующие передачу болевых импульсов. Для местной и проводниковой анестезии используют препараты, которые действуют на периферические нервные волокна, они не оказывают действия на головной мозг и поэтому редко вызывают побочные эффекты со стороны центральной нервной системы.

Во время операции пациент ничего не ощущает благодаря тому, что блокируется передача болевых импульсов
Для общего обезболивания используют наркотические препараты, которые блокируют боль, воздействуя на центры головного мозга. Но препаратов, которые воздействуя на болевые центры мозга, не оказывали бы влияния на другие центры, нет. Поэтому наркоз может делать только специалист-анестезиолог.
Почему возникает тошнота и рвота после общей анестезии
Тошнота и рвота, как следствие наркоза, носят центральный характер, то есть возникают из-за воздействия наркозных средств на структуры головного мозга. Все наркотические препараты, даже те, которые разрешены к применению в медицинской практике, вызывают токсическое действие на головной мозг. Симптоматика может быть следствием интоксикации, а также временной дисфункции вестибулярной системы. Выраженность симптомов зависит от конкретного лекарственного вещества, а также от индивидуальной чувствительности организма. Современные препараты редко вызывают побочные эффекты, что позволяет делать безопасный наркоз даже детям.

Как правило, такая тошнота сопровождается головокружением, усиливается при изменении положения тела, рвота не приносит облегчения. Симптомы проходят самостоятельно через несколько часов. Если наркоз был длительным и глубоким неприятные проявления могут сохраняться несколько дней.
Не всегда симптоматика после операции возникает из-за общего наркоза, так при выполнении операций на брюшной полости, она может быть следствием раздражения брюшины, и развивается в ответ на оперативное вмешательство. Такие симптомы тоже пройдут через несколько дней, по мере заживления операционной раны.
Еще одной причиной рвоты после ингаляционного наркоза, может быть раздражение рецепторов гортани в результате интубации. В таком случае рвотный рефлекс провоцируют раздраженные рецепторы по задней поверхности глотки (примерно тот же механизм присутствует, когда человек пытается вызвать у себя принудительную рвоту). При раздражении гортани голова не кружится, и тошнота может отсутствовать, больше беспокоят позывы на рвоту. Симптомы проходят через несколько дней, можно облегчить состояние, если рассасывать в это время леденцы или использовать спреи, которые применяют для лечения фарингита и тонзиллита. Лучше выбрать препараты с анестетиком.

Тошнота после наркоза обычно вызвана интоксикацией организма анестезирующим средством
Причиной симптомов после общей анестезии может быть побочное действие других препаратов, которые применяются в этот же период лечения, например антибиотики, в таком случае тошнота и рвота будут продолжаться на протяжении всего курса лечения. В отличие от наркозных средств, побочное действие антибиотиков не сопровождается головокружением.
Почему возникают симптомы после эпидуральной и спинномозговой анестезии
Тошнота и рвота после эпидуральной и спинномозговой анестезии тоже являются следствием воздействия препаратов на центры головного мозга. В результате спинальной анестезии анестетик вводится в полости между оболочками спинного мозга, вызывая их раздражение. Также введение дополнительной жидкости в составе анестетика, может привести к изменению внутричерепного давления, незначительные перепады которого чувствительны для человеческого организма. Так как симптоматика развивается в результате воздействия на центральную нервную систему, она может сопровождаться головокружением, особенно при изменении положения тела. Симптомы купируются самостоятельно, как правило, в день операции, но могут длиться и несколько дней.
Причины тошноты и рвоты после спинальной анестезии также могут быть связаны с раздражением брюшины и приемом сопутствующих лекарственных средств.

Также тошнота может быть вызавана приемом лекарственных средств
Применение местной анестезии, как правило, не вызывает центральной симптоматики. Но и после местного обезболивания, также как и после других видов анестезии тошнота, рвота и головокружение могут являться следствием нервного перенапряжения, которым является оперативное лечение и подготовка к нему. Симптомы проходят в день операции, помогает справиться с ними прием успокоительных препаратов.
Как справиться с неприятными симптомами
Неприятные симптомы легкой степени (кружится голова, тошнота) не требуют лечения и проходят самостоятельно. Если же тошнота в следствии общего наркоза сопровождается неукротимой рвотой, это может стать опасным для течения послеоперационного периода, вызвать несостоятельность швов, развитие перитонита, поэтому при такой симптоматике для подавления рвотного рефлекса назначают противорвотные препараты, они блокируют центры головного мозга и помогают снять опасные проявления.
Если и после выписки из стационара голова кружится, и тошнота не проходит длительно, пациента часто рвет, чтобы выяснить, почему это происходит, необходимо обратиться к неврологу. Если причина в дисфункции нервной системы, а также развитии токсической энцефалопатии, невролог сможет подобрать необходимое лечение, чтобы убрать неприятные симптомы.
Если тошнота и головокружение связаны с чрезмерной мнительностью больного, это также сможет выявить невролог, проведя неврологический осмотр. Врач найдет подходящие препараты и для такого случая, а иногда пациенту будет достаточно беседы и подтверждения того, что волноваться не о чем.
Источник
В настоящее время спинальная анестезия (СА) вновь получила широкое распространение, что обусловлена ее простотой и доступностью, способностью надежно блокировать болевую импульсацию, вызывать релаксацию, предотвращать развитие многих нейровегетативных реакций во время операций. Вместе с тем, как и любому другому способу анестезии, СА присущи определенные недостатки. Основной целью настоящей работы являются изучение характера, частоты и причин осложнений и побочных эффектов метода, разработка мер их профилактики.
Материал и методы. Всего СА в качестве анестезиологического пособия во время хирургических вмешательств на органах брюшной полости, малого таза и нижних конечностях использована нами у 2603 больных в возрасте от 10 до 83 лет (1390 мужчин и 1213 женщин). Из них 2265 оперировано в плановом порядке, 338 — по экстренным показаниям. Обезболивание проводили при сохраненном самостоятельном дыхании. Для достижения хирургической стадии СА в 2095 случаях интратекально вводили местные анестетики в чистом виде (2—5 % раствор лидокаина или тримекаина в дозе 1 мг/кг), в 580—наркотические аналгетики (морфин 10—14 мкг/кг или фентанил 0,35—0,7 мкг/кг) в сочетании с 2% раствором лидокаина или тримекаина (1 мг/кг). У 2063 больных использовали изобарические, у 540 — гипербарические растворы местных анестетиков. В случаях интратекального введения наркотических аналгетиков последние из предоперационной подготовки исключали. С целью профилактики артериальной гипотонии 106 пациентам в премедикацию включали 0,5—1 мл 5 % раствора эфедрина; остальным больным непосредственно после интратекального введения обезболивающих препаратов осуществляли умеренную гиперволемическую гемодилюцию. Седативный эффект получали внутривенным введением седуксена (0,07—0,15 мг/кг) или оксибутирата натрия (30—40 мг/кг).
Осложнения и побочные эффекты СА фиксировали на всех этапах лечения больных в стационаре. У 54 больных в возрасте от 52 до 78 лет с патологией органов малого таза и нижних конечностей в предоперационном периоде изучали реакцию сердечно-сосудистой системы на проведение ортоклиностатических проб, используя при этом метод математического анализа ритма сердца [1]. Ретроспективно полученные результаты сопоставляли с гемодинамическими эффектами в ответ на интратекальное введение местно-анестезирующих препаратов.
Результаты исследования и их обсуждение. Из 2603 больных, оперированных под СА различных вариантов, у 2425 (93,2 %) обезболивание было вполне адекватным, у 123 (4,7 %) течение анестезии потребовало дополнительного использования наркотических препаратов и нейровегетативной защиты, у 55 (2,1 %) метод оказался несостоятельным. Недостаточная эффективность или несостоятельность СА были обусловлены тактическими просчетами и техническими погрешностями при выполнении метода.
Осложнения и побочные эффекты СА зарегистрированы нами у 955 (36,7 %) больных, из них у 161 отмечены 2—3 осложнения одновременно, иногда на разных этапах лечения. Сведения об осложнениях и побочных эффектах при использовании различных вариантов СА представлены в таблице.
К осложнениям СА мы относим кратковременную или длительную артериальную гипотонию (снижение АД более чем на 40 мм рт. ст.), выраженную депрессию дыхания и кровообращения (высокий спинальный блок), неврологические последствия СА (головная боль, очаговые неврологические нарушения), а также раннюю и позднюю респираторную депрессию, связанную с интратекальным введением наркотических аналгетиков; побочными эффектами считаем тошноту и рвоту, транзиторные расстройства мочеиспускания, кожный зуд. Снижение АД в пределах 20—40 мм рт. ст. Общая характеристика осложнений и побочных эффектов СА мы рассматриваем как естественное проявление физиологического действия СА.
Общая характеристика осложнений и побочных эффектов СА
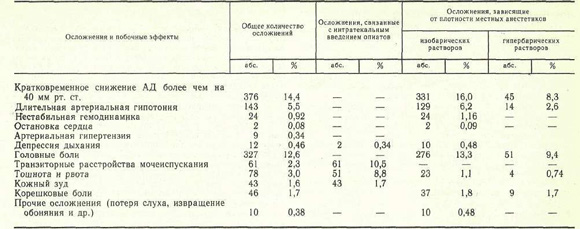
Во время оперативного вмешательства осложнения СА зарегистрированы у 552 (21,2 %) больных, причем при плановых операциях они наблюдались значительно реже (22 % ) , чем при оперативных вмешательствах, выполненных по экстренным показаниям (42 % ) . К наиболее частым интероперационным осложнениям СА следует отнести кратковременную или длительную артериальную гипотонию, причину которой мы склонны видеть в завышении дозы местноанестезирующих препаратов (свыше 1 мг/кг), форсированном их введении в спинномозговой канал, тактических ошибках, связанных с недооценкой анестезиологом плотности местных анестетиков, а также нераспознанной исходной гиповолемией различного происхождения.
Анализируя причины гемодинамических нарушений, мы обнаружили определенную зависимость частоты этого осложнения от уровня люмбальной пункции и возраста больных. Так, при пункции спинномозгового канала на уровне L4 — L5 артериальная гипотония зарегистрирована в 1,7 % случаев, Lз — L4 — в 18,1 %, L2 — L3 — в 44,7 %.
Обращает на себя внимание резкое увеличение количества гемодинамических нарушений (48,9 %) у лиц старше 50 лет, что, на наш взгляд, связано с повышением в этом возрасте числа сопутствующих заболеваний, а также возрастным снижением резервных возможностей организма. Изложенное выше подтверждают дооперационные исследования реакций сердечно-сосудистой системы на проведение классических проб с изменением положения тела. В случаях адекватной реакции с сохранением тонуса сосудов СА не сопровождалась артериальной гипотонией. При исходных неудовлетворительных адаптационных возможностях сердечно-сосудистой системы (скрытая сердечно-сосудистая недостаточность) выраженная и стойкая гипотензия в ответ на интратекальное введение местноанестезирующих препаратов была закономерным явлением и трудно поддавалась коррекции.
Высокий спинальный блок зарегистрирован в 10 (0,38 %) наблюдениях, проявлялся выраженной респираторной депрессией, стойкой и длительной артериальной гипотонией, прогрессирующей брадикардией. У 2 (0,08%) больных он осложнился остановкой кровообращения. Немедленно проведенные реанимационные мероприятия у 9 пациентов позволили восстановить адекватное кровообращение, дыхание, тонус периферических сосудов, а у 1 (0,04 %) больного они не дали эффекта. Причину этого грозного осложнения мы объясняем положением Фоулера на операционном столе после интратекального введения местноанестезирующих препаратов (изобарические растворы), что привело к постепенному распространению анестетика в краниальном направлении с последующей блокадой межреберных нервов, а также соответствующим симпатическим блоком.
Согласно нашим наблюдениям, сроки развития выраженных гемодинамических эффектов были различны. В 47 % случаев артериальная гипотония развивалась через 5—10 мин после интратекального введения местноанестезирующих препаратов, в 48,1 % —через 20—30 мин и только в 0,9 % — в более поздние сроки. Развитие артериальной гипотензии через 20—30 мин и в более поздние сроки можно объяснить фактом окончательной фиксации местноанестезирующих препаратов соответствующими структурами спинного мозга в течение 20 мин [3, 5]. Иначе говоря, местные анестетики, введенные в спинномозговой канал, при определенных условиях (соответствующий угол наклона операционного стола) способны еще в течение довольно длительного времени после развития хирургической стадии СА на нужном сегментарном уровне распространяться в краниальном направлении, блокируя все новые и новые спинальные сегменты. Поэтому для профилактики высокого спинального блока следует рекомендовать тщательный контроль (через каждые 1—2 мин) за уровнем АД, частотой пульса, уровнем блокады болевой чувствительности в течение первых 20—30 мин. Обращает на себя внимание значительное уменьшение числа случаев артериальной гипотензии при использовании гипербарических растворов (см. таблицу). Согласно нашим наблюдениям, СА гипербарическими и особенно вязкими растворами (на 8—10 % растворе глюкозы) в положении с умеренно, опущенным ножным концом стола на период фиксации анестезирующих препаратов позволяет блокировать строго ограниченное количество спинальных сегментов, а следовательно, и симпатических нервных стволов и сплетений.
Наиболее эффективным мероприятием по предупреждению артериальной гипотонии мы считаем переливание в течение 10—15 мин после интратекального введения обезболивающих препаратов коллоидно-кристаллоидных растворов в объеме 10—15 мл/кг с последующей инфузионно-трансфузионной терапией в умеренном темпе. Включение в премедикацию эфедрина и других вазопрессоров, на наш взгляд, не всегда оправдывает себя, а в ряде наблюдений провоцирует артериальную гипертензию, особенно у больных с сопутствующей артериальной гипертонией. Так, стойкая артериальная гипертензия зарегистрирована нами у 9 из 106 пациентов, получивших в премедикации эфедрин, что составило 8,5 %. Полагаем, что использование вазопрессоров оправдано только при резком снижении АД и неэффективности инфузионной терапии1.
Осложнение, связанное с интратекальным введением наркотических аналгетиков, зарегистрировано только у одного больного. Это была респираторная депрессия, связанная с ошибочным введением в спинномозговой канал 2 мл 0,005 % фентанила в сочетании с 2 % раствором лидокаина (1 мг/кг). Осложнение развилось через 10 мин, устранено вспомогательной ИВЛ в течение 20 мин. Исход благоприятный.
В ближайшем послеоперационном периоде осложнения и побочные эффекты СА отмечены у 451 (17,7 %) больного. К наиболее частым осложнениям следует отнести головные боли — у 327 (12,6%) больных: У 225 (78 %) пациентов они были умеренными и продолжались не более 1—2 дней. В 72 (22 %) наблюдениях зафиксированы стойкие и длительные головные боли (продолжительностью 3—5 дней и более). Как правило, это осложнение развивалось у лиц молодого и среднего возраста и значительно реже у пожилых людей и стариков (25,9 % ). Считают [3, 6], что патофизиологической основой головных болей являются прокол твердой мозговой оболочки и связанная с ним ликворея. Следуя этой точке зрения, легко объяснить вышеизложенный факт ранним активным поведением людей молодого возраста (переход в вертикальное положение), провоцирующим увеличение ликворного давления в спинномозговом канале, а следовательно, и большую потерю спинномозговой жидкости. Профилактические мероприятия — строгий постельный режим в течение 24 ч, положение на животе, внутривенное введение изотонических солевых растворов — позволили значительно снизить частоту постпункционных головных болей.
Другие неврологические осложнения в виде корешковых болей, явлений межостистого лигаментоза, преходящих нарушений обоняния и слуха были зарегистрированы у 56 (2,1 %) больных.
Поздняя респираторная депрессия отмечена у одного больного через 8 ч после интратекального введения 3 мг морфина (37 мкг/кг) в сочетании с 2 % раствором лидокаина (80 мг). Операция иссечения геморроидальных узлов и анестезия прошли без осложнений. В удовлетворительном состоянии со стабильными показателями гемодинамики и функции внешнего дыхания больной переведен в палату. Респираторная депрессия развилась внезапно, без каких-либо предвестников на фоне относительного благополучия и полного отсутствия боли. Осложнение проявилось в урежении дыхания до 4—5 в минуту, диффузном цианозе и потребовало ИВЛ в течение 8 ч. Исход благоприятный. Причину поздней респираторной депрессии мы склонны объяснить длительной задержкой наркотического аналгетика и его метаболитов в спинномозговой жидкости и мозговой ткани с последующим депрессивным воздействием на дыхательный центр. Превышение стандартной дозы морфина более чем в 3 раза способствовало развитию данного осложнения.
Побочные эффекты СА в виде тошноты и рвоты, транзиторной задержки мочеиспускания, кожного зуда в преобладающем большинстве случаев сопровождали интратекальное введение наркотических аналгетиков, чаще морфина (см. таблицу). Тошнота и рвота возникли у 78 (3 %) больных в ближайшие 2 ч после операции, преимущественно у женщин и ослабленных больных, а также в случаях завышения стандартных доз опиатов, введенных интратекально. Транзиторные расстройства мочеиспускания зарегистрированы у 61 (2,3%) больного и не требовали специального лечения. Кожный зуд отмечен у 43 (1,7 %) пациентов, исчезал самостоятельно или после введения антигистаминных препаратов. Механизмы развития перечисленных выше побочных эффектов подробно описаны в литературе [2—4].
Таким образом, СА при грамотном ее выполнении — достаточно безопасный метод обезболивания при условии пункции спинномозгового канала на уровне L2 — L5 Степень выраженности отрицательных гемодинамических эффектов зависит от зоны распространения спинального блока и резко увеличивается при «высокой» СА. Наиболее опасные осложнения СА — высокая спинальная блокада и поздняя респираторная депрессия. Большинство осложнений СА связаны с погрешностями в технике и методике ее выполнения, недооценкой значимости профилактических мероприятий, направленных на предупреждение артериальной гипертензии и высокого спинального блока. Анализ полученных данных позволил нам выделить группу повышенного риска, в которую входят лица пожилого и старческого возраста, больные с выраженной гиповолемией различной этиологии, неудовлетворительными компенсаторными возможностями сердечно-сосудистой системы (скрытая сердечнососудистая недостаточность).
ВЫВОДЫ
- При проведении СА следует неукоснительно соблюдать все существующие правила ее выполнения с обязательным учетом плотности вводимых интратекально препаратов.
- СА наиболее безопасна при операциях на органах малого таза и нижних конечностях. Использование СА при оперативных вмешательствах
на органах верхней части брюшной полости представляет реальную опасность из-за резкой артериальной гипотонии и респираторных
нарушений. - Оптимальная доза лидокаина (тримекаина) для интратекального введения составляет 1 мг/кг, морфина — 10 мкг/кг, фентанила — 0,35 мкг/кг.
- У лиц, относящихся к группе повышенного риска, от СА следует отказаться в пользу другого метода обезболивания.
ЛИТЕРАТУРА
- Рифтин А. Д., Гельцер Б. И., Григоренко Г. Ф. Распознавание функциональных состояний организма на основе кибернетического анализа сердечного ритма: Метод, разработка. — Владивосток, 1986.
- Хапий X. X., Давыдов С. Б. Современные методы регионарной анестезии: Осложнения, их профилактика и лечение: Обзор, инофрм.— М., 1988.
- Covino В. G. I/ Int. Anesth. Clin.— 1989.—Vol. 27, N 1.— P. 8—12.
- Duthie D. J., Nitnmo N. S. // Brit. J. Anaesth,— 1987.— Vol. 59, N 1.—P. 61—77.
- Francois Q., Cara M., Deleuze R., Poisvert M. Medecine L’urgence Anesthesia Reanimation Pares.— 1981.— Vol. 8.— P. 136—143.
- Lambert D. H. // Int. Anesth. Clin,—1989.—Vol. 27, N 1. P. 51—55.
1 В 1988 г. в журнале «Anesthesiology» № 1 A. Keats, анализируя случаи внезапной остановки сердца во время СА, пришел к выводу, что все они — результат артериальной гипотензии из-за резкой вазоплегии и применение вазопрессоров (адреналина), а не инфузионная терапия должно быть первоочередным жизнеспасительным мероприятием.— Прим. ред.
Источник
